Dans notre article du 22 avril dernier, nous vous disions avoir interpellé la Direction Générale de la santé concernant les malades thyroïdiens toujours sous l'alternative Euthyrox.
Une date butoir avait été posée par le Laboratoire Merck, septembre 2020 soit dans 5 mois, en dépit de la mobilisation de tous ceux qui voulaient récupérer cette formule équivalente au Levothyrox au lactose.
Si beaucoup de malades, las de se battre et désireux de retrouver la santé, se sont tournés vers les alternatives disponibles, ce sont encore 122 000 usagers qui achètent l'Euthyrox en France ( chiffres officiels de la DGS).
Une commission d'encadrement avait été mise en place en octobre afin d'accompagner les malades vers les autres spécialités disponibles.
Les associations de patients, unanimement, avaient dénoncé l'arrêt d'une formule au lactose qui convient à tant de patients et avaient tenté de garder cette alternative.
En avril, l'UPGCS attirait l'attention des autorités sur une période peu propice à un changement :
- Le confinement a rendu impossible toute réunion d'informations sur la disparition de cette spécialité, notamment pour les nombreux malades thyroïdiens qui n'ont pas accès à l'information numérique.
- Actuellement, l'épidémie de Covid-19 complique les possibilités de consultations spécialisées, les rendez-vous ayant été reporté pendant le confinement, augmentant les délais d'attente.
- Nos associations sont submergées d’appels de détresse de malades qui ne peuvent faire renouveler leurs ordonnances en raison de la pénurie de cette spécialité .Rappelons que nous sommes dans le cadre d’un médicament à marge thérapeutique étroite qui ne peut être substitué sans encadrement.
- Les associations avaient soulevé des objections sur les documents destinés aux malades et aux professionnels de la santé, pour préparer et encadrer au mieux la transition vers les alternatives de T4. Nous n'avions donc ni validé ces documents ni les supports de leur diffusion.
C'est face à ce constat que nous demandions un report d'échéance auprès du laboratoire Merck et auprès de la DGS.
Malheureusement, le couperet est tombé, la date de septembre reste maintenue !
https://www.upgcs.org/2020/04/22/malades-thyro%C3%AFdiens-sous-euthyrox-au-lactose-et-covid-19/
La réponse de Jérôme Salomon, Directeur Général de la Santé
Réponse de Valérie Leto, Directrice générale et pharmacien responsable auprès du laboratoire Merck Serono
Mesdames,
Nous revenons vers vous au sujet de votre demande de prolongation de mise à disposition d’Euthyrox® au-delà de septembre 2020.
Cette décision ne nous appartient pas et nous ne doutons pas que vous recevrez sous peu une réponse des autorités compétentes.
Nous nous permettons toutefois d’attirer votre attention sur le risque de remise en cause d’un calendrier validé depuis plusieurs mois maintenant, toujours délicate sur des productions et des chaines logistiques sophistiquées comme celles du secteur pharmaceutique, déjà mises à rude épreuve par la situation créée par le COVID-19.
Comme vous le soulignez en effet, la coordination dans la perspective d’une fin de mise à disposition d’Euthyrox® a été engagée dès le mois d’octobre 2019 par les autorités de santé, sous le pilotage de la Direction Générale de la Santé. En janvier 2020, le calendrier retenu a posé la date de septembre 2020 et toutes les parties prenantes ont acté du principe d’un accompagnement renforcé des patients concernés dans les mois qui précédent. Il est en effet dans l’intérêt des patients sous Euthyrox® d’effectuer leur transition vers une alternative thérapeutique pérenne dès que possible et sous le contrôle de leur médecin, comme cela a été rappelé dès le 8 janvier 2020 dans le communiqué de presse du ministère de la santé :
« Par ailleurs, les autorités sanitaires recommandent aux prescripteurs de ne plus initier de traitement par Euthyrox®. En cas de renouvellement de prescription, le médecin doit informer son patient et anticiper avec lui l’évolution du traitement. »
A ce stade et conformément à la demande qui nous a été faite, les boîtes d’Euthyrox® mises sur le marché à partir du mois de mai annonceront donc l’échéance de septembre 2020. Or, nous ne pouvons pas prendre le risque de ne pas mettre ces boîtes sur le marché car cela entraînerait un double préjudice pour les patients : une diminution de la disponibilité et, de surcroît, une longue période de rupture.
Concernant le plan et les supports de communication destinés à accompagner les patients et les professionnels de santé durant cette phase, nous n’avons pas participé au groupe de travail et restons dans l’attente de leur diffusion.
Nous partageons votre volonté d’agir dans le meilleur intérêt des patients et pouvons vous assurer que nos équipes sont pleinement mobilisées pour faciliter leur transition.
Veuillez accepter, Mesdames, l'expression de mes salutations distinguées.
Valérie Leto
Pharmacien Responsable Merck Serono et Directrice Générale
Notre réponse consécutive à ces décisions
Nos réf. : D-206008685
Vos réf : votre réponse du 14 mai 2020
A Monsieur Jérôme Salomon, Directeur Général de la Santé
Monsieur,
C’est avec beaucoup de désillusion que nous prenons acte de votre réponse concernant un simple report de la fin de mise à disposition de l’Euthyrox.
Ceci nous amène à vous proposer quand la crise sanitaire majeure Covid-19 sera résolue, de mettre en place un grand chantier de réflexion sur le rôle réel joué par les associations de patients dans les consultations au sein de la DGS.
La commission d’encadrement de la fin de l’Euthyrox démontre en effet qu’aucune des demandes des associations n’a été entendue, ni celles concernant l’intérêt du maintien d’une spécialité qui convenait à beaucoup de malades, ni la demande de report de cette date puisque nous n’avons pas été en mesure d’organiser les réunions d’information nécessaires aux malades sans accès internet (confinement Covid), ni même sur le document d’accompagnement qui devait recevoir notre accord définitif avant validation finale.
Dans les biologies post changement de traitement, L’observation des T3L (qui avait pourtant obtenu un avis favorable) a complètement disparu des recommandations.
Nous nous retrouvons donc dans la situation de 2017, avec une substitution de formule lévothyroxine imposée contre l’avis des associations de patients et sous les mêmes recommandations de surveillance qui ont démontré leur inefficacité depuis 2017, au regard du nombre impressionnant de malades thyroïdiens toujours en déséquilibre 3 ans plus tard.
Comme évoqué dès notre courrier d’octobre, les mêmes causes produiront les mêmes effets, et notamment en termes de confiance perdue vis-à-vis des décisions prises concernant la santé des usagers.
Plusieurs fois, l’UPGCS a suggéré que si la fin de disposition de l’Euthyrox était inévitable, ce passage obligé à des alternatives soit l’occasion d’une communication forte envers des malades bafoués en 2017, afin que médecins et endocrinologues soient attentifs aux répercussions des changements de traitements et ne soient plus porteurs de ce type de messages « Votre TSH est bonne, c’est dans votre tête ». (témoignages reçus d’adhérents après des consultations de février 2020 ! ). Il n’en sera rien, les documents ayant été communiqués par mail aux médecins et pharmaciens dès janvier, avec l’impact qu’on connaît quant à ce type de communication.
C’est donc avec la plus grande amertume quant au rôle réel des nos associations et à l’intérêt porté à la parole des malades, que nous prenons acte et que nous communiquerons vos décisions à l’ensemble de nos adhérents. L’information sera sur notre site dès ce jour avec l’ensemble des documents mais également nos échanges de courrier afin de communiquer sur notre analyse finale après des mois d’échanges et de travail vain …
Nous vous prions Monsieur le Directeur, d’accepter l’expression de notre respect quant aux obligations qui sont les vôtres en cette période de pandémie.
Pour l’UPGCS,
Annie Notelet et Elise Carboullec
Arrêt de distribution de Euthyrox. Document d'accompagnement à la substitution du traitement à base de lévothyroxine

Recommandations à l'usage des patients et des médecins pour faciliter le passage à une alternative
La distribution de Euthyrox®, en France, s’arrêtera en septembre 2020.
Dans ce cadre, vous trouverez ci-dessous des recommandations à l’attention des patients et professionnels de santé pour accompagner les patients actuellement sous EUTHYROX® à un changement de traitement vers une autre spécialité à base de lévothyroxine.
Toutes les spécialités proposées sur le marché contiennent la même hormone, la lévothyroxine. Les différentes spécialités disponibles en France avec leurs différentes compositions (excipients) sont commercialisées également à l’étranger depuis plusieurs années.
Les effets indésirables signalés peuvent avoir différentes causes, notamment le fait que la dose doit être adaptée au patient.
C’est pourquoi chaque changement de formule ou de spécialité peut affecter
l’équilibre des hormones thyroïdiennes et nécessiter un réajustement.
Votre médecin, votre pharmacien et votre infirmier vous accompagneront pour répondre à vos questions et vous aider à passer cette période de transition où des effets indésirables peuvent apparaître.
Le rééquilibrage peut prendre entre quelques semaines et plusieurs mois avec le même traitement et doit faire l’objet d’un accompagnement particulier de la part des professionnels de santé.
Votre traitement ne vous expose pas à un risque accru de contracter le virus responsable du COVID-19.
Par conséquent, vous ne devez pas arrêter votre traitement substitutif par levothyroxine.
Son arrêt vous exposerait à une récidive des symptômes d’hypothyroïdie ou d’hyperthyroïdie.
Recommandations aux professionnels de santé
Ne plus initier de traitement par EUTHYROX® afin de ne pas exposer les patients à un changement imminent de traitement.
Organiser un changement de traitement pour vos patients pour lesquels vous avez continué à prescrire de l’EUTHYROX®.
Il est nécessaire de changer de traitement au plus tôt afin de vous laisser un temps suffisant pour ajuster les posologies et permettre au patient de s’habituer à son nouveau traitement.
A noter que les patients ayant une hypothyroïdie centrale, les enfants, les femmes enceintes, les patients souffrant de problèmes cardiovasculaires et ceux ayant subi une thyroïdectomie pour cancer thyroïdien avec impératif de freinage de TSH doivent relever d’une consultation par un endocrinologue (pour les autres problématiques de santé rencontrées, le suivi continuera d’être assuré par le spécialiste référent).
Un carnet de suivi du traitement par levothyroxine, destiné à être rempli par le patient et son médecin et à permettre le recueil d’informations essentielles dans le cadre du parcours de soin du patient est à votre disposition pages 10, 11 et 12.
Ce changement de traitement doit suivre trois étapes.
ETAPE 1 - Avant la prescription d’une alternative à EUTHYROX®
- Recueillez les données permettant d’établir l’état de santé du patient (antécédents, constantes, symptômes, le cas échéant) à l’aide du tableau du carnet de suivi des pages 10, 11 et 12.
- Informez le patient des différentes alternatives existantes (cf.page 9 « Médicaments à base de lévothyroxine disponibles en France en février 2020 »). A noter qu’EUTHYRAL® est une association fixe de lévothyroxine (LT4 : 100 µg/comprimé) et de liothyronine (LT3 : 20 µg/comprimé) et ne peut se substituer à EUTHYROX®. EUTHYRAL® n’est pas indiqué dans le cancer de la thyroïde. Il est déconseillé chez les femmes enceintes et doit être évité chez les patients atteints de cardiopathies.
- Expliquez au patient qu’un changement de traitement par hormones thyroïdiennes peut nécessiter un rééquilibrage des posologies d’hormones pouvant nécessiter quelques semaines à plusieurs mois avec ce même traitement et qu’il doit faire l’objet d’un accompagnement personnalisé.
- Demandez au patient de faire un dosage biologique.
Si l’état clinique du patient sous EUTHYROX® est satisfaisant, le dosage de TSH est suffisant pour déterminer la valeur cible pour ce patient.
Si son état n’est pas cliniquement satisfaisant, il est préférable de faire pratiquer un dosage de TSH et de T4 Libre (T4L) pour connaitre la marge d’ajustement de posologie.
Tenez compte de la préférence du patient et de son expérience si des changements de traitement à base de lévothyroxine ont déjà eu lieu pour choisir l’alternative qui semble la mieux adaptée (spécialité, forme pharmaceutique, remboursement…). Voir logigramme 1.
- Conservez la posologie habituelle en population générale.
- Pour les patients à surveillance particulière (patient ayant une maladie cardiaque, respiratoire, digestive, personnes âgées, mauvaise tolérance du Lévothyrox® nouvelle formule avec signes d’hyperthyroïdie), diminuez légèrement la posologie pour éviter le surdosage (risque du surdosage versus inconfort du sous-dosage).
- Prescrivez un dosage de TSH que le patient fera réaliser 6 à 8 semaines après le changement de traitement. Si son état de santé n’était pas satisfaisant sous Euthyrox® prévoir un dosage de TSH et T4L 6 semaines après le changement de traitement. Appréciez au cas par cas l’intérêt des autres dosages. Voir logigramme 2.
- Rappelez au patient de ne pas arrêter ou modifier son traitement sans avis médical.
En cas d’effet indésirable, ne pas oublier de faire une déclaration de pharmacovigilance Ceci est très important afin de permettre la surveillance de tous les médicaments.
Lien du portail des vigilances : https://signalement.social-sante.gouv.fr/


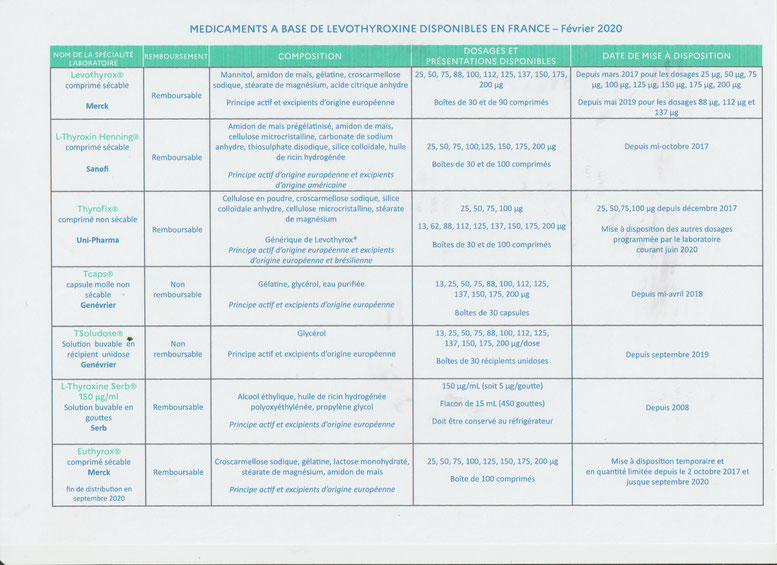
Dans ce PDF, vous retrouverez toutes les fiches d’accompagnement, à l'usage des patients et des médecins, la liste des alternatives et le dossier de suivi des malades thyroïdiens pour y noter vos différents changements de traitements et les résultats des biologies.
Nous ne pouvons que vous conseillez de télécharger ces documents et de les partager avec vos médecins afin de gérer au mieux votre switch.
Nous rappelons que ces documents officiels ne prennent pas en compte les recommandations sur l'optimisation de la transformation des T4 en T3, par l'apport de vitamines indispensables. ( se référer à notre article https://www.upgcs.org/2020/02/08/levothyroxine-m%C3%A9dicament-%C3%A0-marge-th%C3%A9rapeutique-%C3%A9troite-mieux-en-comprendre-les-usages/)
Le 29 mai prochain, l'UPGCS sera en vidéo conférence HAS ( Haute Autorité de Santé) pour tenter de faire évoluer la prise en charge des dysthyroïdies. Nous aurons à nos côtés pour soutenir ce dossier le Docteur Didier Cosserat et le Docteur Mohamed Boutbaoucht. Observer les malades au travers du facteur TSh est obsolète et le scandale Levothyrox de 2017 en est révélateur.
Elise Carboullec et Annie Notelet pour l'UPGCS
La complexité de cet article, qui appellera des réponses individuelles nous amène à bloquer les commentaires par souci d'efficacité. Merci de nous les adresser par mai à : upgcs.direction@gmail.com
Merci à vous.


